手性是生物分子的基本特征,在氨基酸、糖类等基本结构单元中普遍存在。DNA的右手双螺旋与蛋白质的右手α-螺旋等螺旋结构作为手性的重要表现形式,在遗传信息传递、转录调控以及酶的立体专一性催化等生命过程中扮演着不可替代的关键角色。受此类生物分子手性结构的影响,使得手性分子的一对对映异构体往往表现出显著的生物活性差异,通常一个对映体具有疗效,而另一个则无效或产生不良反应。采用手性固定相(CSPs)的高效液相色谱(HPLC)技术是获取单一对映体最常用的方法。然而,实现不同尺寸和手性外消旋体的基线分离仍是一项艰巨的挑战。
基于此,吴宗铨教授团队通过钯催化活性聚合合成了端基带有巴比妥酸单元的左手和右手螺旋聚异腈,并利用其与三官能Hamilton楔形分子的氢键自组装,构建了一系列具有规整六边形孔道的手性聚异腈框架(图1)。通过精确调控聚异腈的聚合度,实现了框架孔径从2.62 nm至8.63 nm的线性调控;通过调控单体手性,可控制框架的整体手性。该框架作为手性固定相和分离膜,成功拆分了20种不同尺寸和手性的外消旋小分子及聚合物。研究表明,分离因子取决于孔径与对映体尺寸的匹配度,而对映体洗脱顺序则由框架手性决定。
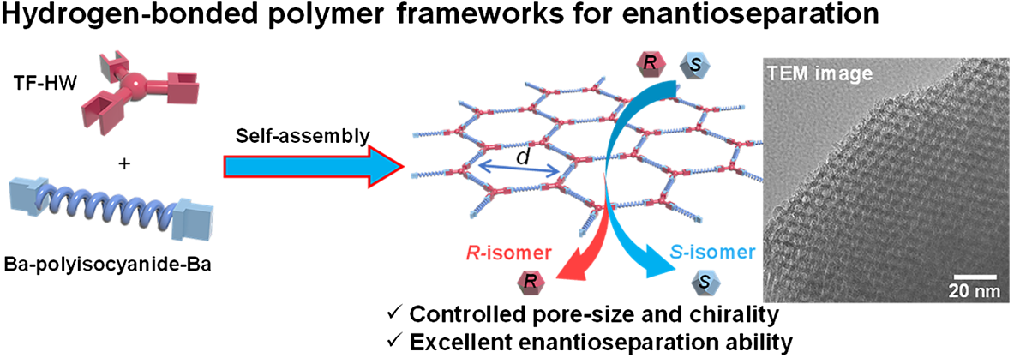
图1.手性聚异腈框架用于不同尺寸和手性外消旋体的对映体分离
相关研究成果“Polymer Frameworks with Controllable Pore Size and Chirality for Enantioseparation of Racemates with Different Sizes and Chiralities”为题发表在CCS Chemistry上(DOI:10.31635/ccschem.026.202506825),文章第一作者为吉林大学高润檀博士,吉林大学吴宗铨教授为论文通讯作者。
论文链接:
//www.chinesechemsoc.org/doi/10.31635/ccschem.026.202506825